➀ Kalkulator on-line Komornik©⇒ dawka emitowana, dostarczana i deponowana z wykorzystaniem pMDI z komorą inhalacyjną: uwagi ogólne. ➁ Opis kontrolek kalkulatora, czyli co trzeba wiedzieć, by wypowiadać się na temat metody leczenia. ➂ Uwagi na temat parametrów sprzętu w metodzie pMDI. ➃ Małe dziecko jako podmiot terapii w metodzie pMDI+KI. ➄ Maseczka jako element szczególny w metodzie leczenia z wykorzystaniem pMDI i KI. ➅ Model sekwencyjnego poboru aerozolu z KI. ➆ Model poboru aerozolu z KI uwzględniający dyfuzję. ➇ Podsumowanie algorytmu i wnioski. ▷
W dyskusjach toczonych wokół problematyki kalkulacji dawek w nebulizacji wielokrotnie przewija się motyw krytyki dużej liczby i znacznego stopnia komplikacji parametrów koniecznych do uwzględnienia przy kalkulacji dawki dostarczanej i deponowanej z inhalatora ciśnieniowego pracy ciągłej. Zdawać się może, że jeden z argumentów za wyborem alternatywnych metod leczenia, to jest ich prostota, jest słuszny i racjonalny. Słuszność takiego rozumowania jest jednak złudna i pozorna: oto dyskusje na temat porównywania metod leczenia prowadzimy na gruncie znacznego postępu teorii i praktyki racjonalniej nebulizacji. Rodzi się zatem pytanie, czy metoda leczenia oparta na urządzeniach pMDI jest na pewno prosta, czy też może, (podobnie jak nebulizacja przed kilkoma laty) nie doczekała jeszcze momentu poprawnego opisu zjawisk i rządzących nie prawideł.
Przy powierzchownym postrzeganiu rzeczywistości niektóre otaczające zjawiska i rzeczy jawią się z jednej strony jako banalnie proste, z drugiej strony natomiast jako niezrozumiałe i tajemnicze. Ten odwrotnie proporcjonalny związek można w uproszczeniu sprowadzić do stwierdzenia, że głębszej dociekliwości, szerszym horyzontom wiedzy i większej skali komplikacji pojęć towarzyszy bardziej krytyczna percepcja. Świat postrzegany w nowy sposób nie jest już tak naiwnie prosty, jednak w zamian staje się mniej tajemniczy, staje się bardziej racjonalny. Leczenie z wykorzystaniem pMDI w powszechnym rozumieniu jest banalnie proste: wyzwalamy i podajemy pacjentowi dawkę leku. Z drugiej strony leczenie z wykorzystaniem pMDI skrywa wiele tajemnic: u jednego chorego daje dobre efekty, u innego niezadowalające. To dziwne i tajemnicze. Dlaczego współczesna medycyna w przypadku astmy nie dysponuje do chwili obecnej danymi opisującymi prostą zależność dawka – odpowiedź na leki przeciwzapalne? Wystarczy jedne rzut oka na tabele dawek zalecanych by głęboko zastanowić się na przyczynami, z powodu których rozstęp dawek terapeutycznych jest tak kolosalny. Pierwsza myśl, jaka się nasuwa to ta, że astma jest chorobą tajemniczą, czytaj: nieznaną. To nieprawda. O astmie wiemy bardzo wiele od badań epidemiologicznych począwszy aż po subtelne różnice w konformacji białek receptorów poznawane na poziomie molekularnym. Druga możliwość to nieskuteczne preparaty terapeutyczne. To nieprawda. W badaniach udowodniono skuteczność leków. Może zatem tych skutecznych leków nie potrafimy poprawnie podać?
Dokonajmy próby rzetelnej analizy techniki leczenia z wykorzystaniem dozowników pMDI z komorami inhalacyjnymi. Nazwijmy i zinterpretujmy konkretne zjawiska, zdefiniujmy kluczowe parametry i zadajmy pytania o naturę ich wzajemnych zależności. Zadajmy wspólnie kardynalne pytania o relacje między podmiotem terapii za konstelacją czynników tworzonych przez układ dozownika ciśnieniowego, komory inhalacyjnej i maseczki. Wreszcie, co jest niezwykle istotne, porównajmy rzetelność informacji na temat parametrów technicznych urządzeń pMDI i komór inhalacyjnych z informacjami dostępnymi w instrukcjach obsługi nebulizatorów.
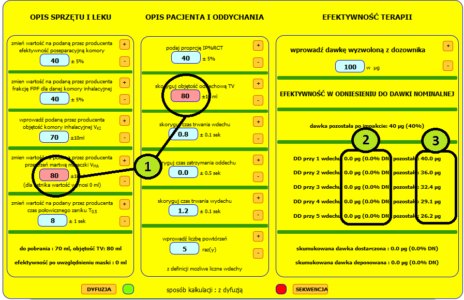
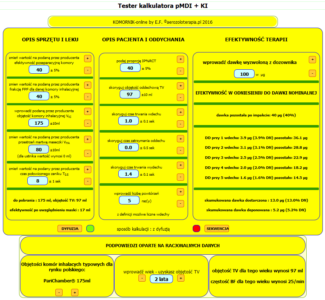
Ryc 1. Układ kontrolek kalkulatora dawek dostarczanych z pMDI+KI.
Rycina 1 przedstawia konsolę kalkulatora dawkowania KOMORNIK©. Kontrolki uszeregowano w trzech kolumnach: w kolumnie 1 należy dokonać opisu zastosowanego urządzenia. W kolumnie 2 ustawić należy podstawowe parametry opisujące sposób oddychania pacjenta oraz dodatkowo technikę wykonywania inhalacji. Antycypowaną efektywność terapii podają komunikaty ujęte w kolumnie 3. Jak wiadomo (szczegóły w artykule o aerozolu z pMDI), w zależności od ciśnienia par nośnika strumień cząstek „wystrzeliwany” jest do otoczenia z różną prędkością. Przy zastosowaniu komory inhalacyjnej na jego drodze pojawia się przeszkoda: przeciwległa ściana komory, co pociąga za sobą konsekwencje w postaci depozycji inercyjnej. Przy nebulizacji stałe ciśnienie robocze inhalatora oraz przepływy są podawane przez producenta. W technikach pMDI producent nie podaje żadnych danych możliwych do wykorzystania przy oszacowaniu skali zjawisk depozycyjnych: zależności ciśnienie-temperatura ani zależnych od nich prędkości liniowych aerozolu. Producenci komór nie podają wymiaru podłużnego komory, co byłoby użyteczne przy oszacowaniu drogi, po której aerozol uderza w ścianę komory. Wiadomo jednak, że zjawiska inercyjne zachodzą „w-jakimś-tam-stopniu” a sprawność po-separacyjna komory (4) rozumiana jako liczbę cząstek/objętość aerozolu przetrwałą po kataklizmie impaktu „jkaś-tam-jest„. Zadaniem użytkownika jest podanie na podstawie głębokiej wiary, wróżby z kart, horoskopu a najlepiej zdroworozsądkowego domysłu (bo nie na podstawie opublikowanych przez producenta danych) tejże „jakiejś-tam” wartości. Autor kalkulatora, na podstawie obserwacji zachowania farby w sprayu jest przekonany, że ponad 90% aerozolu „wystrzelonego” w kierunku ściany musi nieuchronnie zdeponować się na ścianie (do tego służy farba w sprayu). Na potrzeby kalkulacji start z pMDI przyjęto bardziej optymistyczne założenie: strata wynosi jedynie 60% a sprawność po-separacyjna komory ustawiona jest na 40% (przyciski (+) i (-) pozwalają na ustawienie kontrolki 4 w zakresie 5% do 90%). W kontrolce 17 podawana jest dawka nominalna przetrwała po impakcie ( a konkretnie jej procent).
Kontrolka 5 służy do ustalenia udziału frakcji cząstek drobnych (FPF) w ogólnej masie przetrwałego aerozolu. Niestety, producent dozownika pMDI nie podaje tego parametru. Sprawę komplikuje dodatkowo dylemat, czy aerozol w momencie impaktu podlega koalescencji (wzrost MMAD) czy też może re-dyspersji (spadek MMAD)? W zdecydowanie lepszej sytuacji są użytkownicy nebulizatorów, gdzie parametry przepływów, wydatku i przedmiotowej FPF podawane są precyzyjnie. Autor po użyciu wahadełka i różdżki wierzbowej oszacował FPF zawarte w komorze po impakcie na około 40% (przyciski (+) i (-) pozwalają na ustawienie kontrolki 4 w zakresie 5% do 90%).
Objętość komory inhalacyjnej jest jednym z nielicznych parametrów dostępnych w postaci źródłowej, czyli opisanej przez producenta. Kontrolka 6 pobiera automatycznie dane z pola podpowiedzi 22, czyli katalogu KI dostępnych na polskim rynku.
Przestrzeń martwa maseczki jest bardzo istotnym elementem układu podaż-pobór. Jej wartość ustawiamy kontrolką 7. Parametr ten jest bardzo często pomijany milczeniem w dyskusjach nad skutecznością inhalacji z KI, co znajduje odzwierciedlenie w braku ogólnie dostępnych danych źródłowych na temat przestrzeni martwej maseczek.
Aerozol w komorze inhalacyjnej podlega procesom degradacji a miarą jej tempa jest czas połowicznego zaniku aerozolu T0.5. Parametr ten ustawiamy za pomocą kontrolki 8. Obszar 9 pozwala na oszacowanie proporcji objętości podaży, w skład której wchodzi objętość KI i maseczki (suma objętości wprowadzanych do układu oddechowego) do możliwości poboru, czyli objętości pojedynczego wdechu.
Ryc 2. Raport przestrzegający przed oscylacyjnym nieskutecznym poborem z maseczki.
W sytuacji, w której zalecenia ekspertów forsują pMDI z komorą inhalacyjną w najmłodszych grupach wiekowych, w tym u niemowląt i noworodków dramatycznie rośnie rola przestrzeni martwej maseczki jako czynnika determinującego skuteczność terapii. Kalkulator sygnalizuje sytuacje, w których zachodzi oscylacyjne wentylowanie przestrzeni martwej maseczki powietrzem oddechowym bez poboru aerozolu. Na rycinie 2, znacznik 1, przedstawiono zmianę koloru tła kontrolek 7 i 11 sygnalizującą konflikt możliwości poboru i przestrzeni martwej układu. Znacznik 2 na rycinie 2 obrazuje raport wyświetlany w obszarze 18 kalkulatora odnoszący się do poboru dawki. Jak widać pobór jest nieskuteczny. Tymczasem znacznik 3 ryciny 2 świadczy o tym, że dawka aerozolu pozostająca w komorze zimniejsza się z wdechu na wdech. Czy, a jeśli tak, to w jaki sposób można wytłumaczyć ten fenomen?
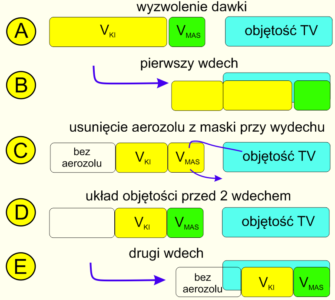
Ryc 3. Przyczyny strat aerozolu w warunkach nieskutecznego, oscylacyjnego poboru z maseczki.
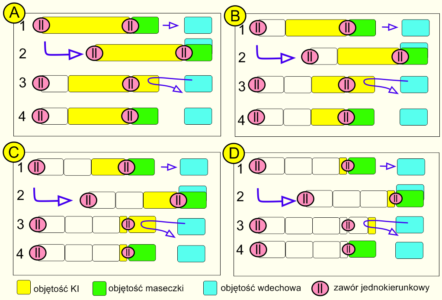
Na rycinie 3 przedstawiono schematycznie zdarzenia w czterech kolejnych wdechach: A, B, C i D. Każdy wdech podzielono na cztery fazy opisane cyframi arabskimi. Znaczenie kolorystyki poszczególnych elementów schematu opisano w legendzie. Początek sekwencji ilustruje sytuacja A1. Aerozol (kolor żółty) zawarty jest w KI między zaworami jednokierunkowymi. W A2 następuje wdech: do niebieskiej objętości oddechowej TV wpada powietrze obecne w maseczce (kolor zielony). Wdech dobiegł końca, ale do dróg oddechowych niemowlęcia nie dotarł aerozol. Na koniec wdechu jak w A3 do komory trafiła objętość powietrza równa objętości pobranej (kolor biały), do maseczki przemieściła się taka sama objętość aerozolu. Niestety, w czasie wydechu zilustrowanego strzałką zwrotną wydychane powietrze usuwa aerozol z przestrzeni martwej maseczki. Rola zaworu zwrotnego ułatwia orientację w zagadnieniu, ale ta zasada jest uniwersalna i działa podobnie w przypadku zwrotnego wydychania powietrza do komory. W efekcie, jak na przykładzie A4, przed drugim wdechem w komorze jest mniej aerozolu, natomiast w maseczce ponownie jest powietrze nieobładowane lekiem. Czwarty wdech D sprawia, że przedmieszczany sekwencyjnie aerozol definitywnie opuszcza komorę inhalacyjną.
Po tej istotnej dygresji powracamy do opisu funkcji kalkulatora w kolumnie 2 tyczącej opisu pacjenta i sposobu wykonywania zabiegu. K0ntrolka 10 opisuje aktualny stopień obturacji, który z kolei wpływa na czas trwania wdechu oraz czas trwania wydechu. Objętość oddechowa TV (11), czas trwania wdechu (12) oraz czas trwania wydechu (14) pobierane są automatycznie po wybraniu wieku pacjenta w polu podpowiedzi 23 z uwzględnieniem wartości kontrolki 10. Sposób kalkulacji jest szczegółowo omówiony w artykułach o cyklu oddechowym pacjenta oraz dawce dostarczane w nebulizacji. Wszystkie omawiane wartości można w szerokim zakresie samodzielnie korygować przyciskami (+) i (-) umieszczonymi obok kontrolek. Noworodki, niemowlęta i małe dzieci nie są w stanie świadomie zatrzymać oddechu, dlatego wartość kontrolki 13 ustawiona jest na 0 sekund. Ostatnia w tej kolumnie kontrolka 15 pozwala na sprawdzanie układu dawek pobranych w zależności od liczby wdechów. Zdaniem autora forsowanie inhalacji liczba oddechów przekradających 5 cykli poboru jest nieracjonalne i tak też ustawiono górna granicę kontrolki.
W kolumnie 3 po ustawieniu w kontrolce 16 dawki nominalnej (wyzwalanej z dozownika do KI) wyświetlane są raporty : o dawce pozostałej w KI po impakcie (17), dawkach jednostkowych przypadających na konkretny wdech po uwzględnieniu czasu połowicznego zaniku aerozolu (18) oraz dawce skumulowanej dostarczonej i dawce skumulowanej deponowanej (19) zliczanych dla zadanej w kontrolce 15 krotności cykli oddechowych.
Kontrolki 20 i 21 pozwalają na zmianę trybu kalkulacji z sekwencyjnego na tryb uwzględniający dyfuzję. Sposób prowadzenia obliczeń i samą koncepcję zagospodarowywania aerozolu z KI w kilku cyklach oddechowych trzeba było na potrzeby kalkulatora „jakoś-tam-nazwać” , pora teraz na wyjaśnienie ich istoty. Przedtem jednak należy uszczegółowić rozróżnienie między objętością komory a objętością układu komora + maseczka.
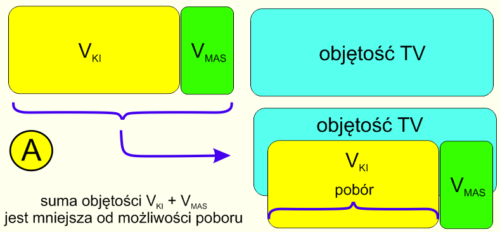
Ryc 4. Założenia teoretyczne dla algorytmu sekwencyjnego poboru aerozolu. Podaż mniejsza od możliwości poboru.
Jak widać na rycinie 4 sytuacja A sytuacja wydaje się prosta. Zdolność do poboru przewyższa sumę objętości KI i maseczki. Nie wchodząc w szczegóły można przyjąć z dużym prawdopodobieństwem, że z taką sytuacją mamy do czynienia u osób dorosłych korzystających z komór nisko objętościowych. Dla tak opisanego układu podaż↔pobór nie jest istotny sposób kalkulacji – jest bowiem pewne, że objętość układu będzie zagospodarowana już przy pierwszym wdechu a konsensusowe zalecenia wykonywania z KI kilku wdechów tracą racjonalne podstawy. Pewne niuanse depozycji można albo pominąć albo ewentualnie dyskutować z wykorzystaniem koncepcji lokalizacji chmury aerozolu w drzewie oskrzelowym.
Ryc 5. Założenia teoretyczne dla algorytmu sekwencyjnego poboru aerozolu. Podaż większa od możliwości poboru.
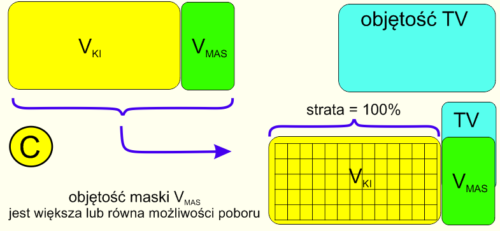
Rycina 5 przestawia sytuację typową dla niemowląt i małych dzieci korzystających z nieodpowiednio dobranych KI. Objętość poboru TV nie wystarcza do pobrania pełnej objętości przestrzeni martwej maski i objętości KI. Po zakończeniu wdechu w komorze pozostaje pewna niezagospodarowana objętość aerozolu i w stosunku do niej rozważamy możliwość obliczeń sekwencyjnych lub obliczeń uwzględniających dyfuzję.
Ryc 6. Założenia teoretyczne dla algorytmu sekwencyjnego poboru aerozolu. Możliwość poboru przez TV jest <= martwej przestrzeni maski.
Rycina 6 przedstawia wyżej omawiany problem maseczki zbyt dużej w porównaniu z objętością oddechową dziecka. Najczęściej z taką sytuacją mamy do czynienia w przypadku konieczności leczenia noworodków i niemowląt. Cały aerozol ulega „przepompowaniu” do otoczenia w omówionym mechanizmie wentylacji oscylacyjnej przestrzeni martwej w maseczce.
Pomysł sekwencyjnego postrzegania poboru sprowadza się do koncepcji, że aerozol tworzy spójny „blok”, z który można „wysuwać” z komory w kierunku dróg oddechowych pacjenta przez ustnik (i ew. zawór wylotowy), a powietrze uzupełniające wprowadzać przez otwór wlotowy ( z ew. zaworem wlotowym). Granica bloków powietrza uzupełniającego i ubywającego aerozolu jest stała.
Ryc 7. Założenia teoretyczne dla algorytmu sekwencyjnego poboru aerozolu.
Schemat ukazany na rycinie 7 ilustruje, że w koncepcji sekwencyjnego poboru wszystkie aspekty losów aerozolu rozpatrujemy z pominięciem dodawanych do układu porcji powietrza uzupełniającego. Mówiąc inaczej: aerozol ma w tym algorytmie stałe stężenie, bowiem ubytek cząstek aerozolu jest proporcjonalny do ubytku jego objętości. W układzie takim liczba wdechów jest z definicji policzalna i równa się ilorazowi objętości podaży i objętości poboru. Algorytm ten zawyża dane dawkowania, ponieważ w sytuacji 7C, 7D i 7E nie zagospodarowana objętość komory traktowana jest jako „pusta”, całkowicie wolna od cząstek aerozolu.
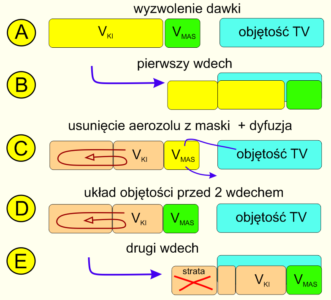
Ryc 8. Założenia teoretyczne dla algorytmu poboru aerozolu z uwzględnieniem dyfuzji.
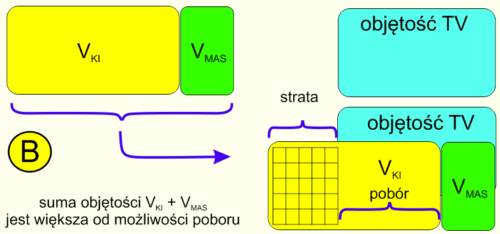
Rycina 8 ilustruje uwzględnienie zjawiska dyfuzji aerozolu do powietrza dopełniającego w algorytmie kalkulacji dawek. W układzie, w którym objętość komory i przestrzeni martwej maseczki jest większa od możliwości poboru przez TV, liczba wdechów jest z definicji niepoliczalna, ponieważ teoretycznie reszta aerozolu pozostała w komorze dyfunduje do powietrza dopełniającego przy stałej objętości układu. Dlatego tak ważne jest w pełni wykonalne dążenie do takiego doboru KI, by pacjent miał szansę na pobranie go w pierwszym wdechu. Pomocna w tym zadaniu może być tabelaryczne zestawienie proporcji objętości oddechowych do objętości popularnych KI. Innym słowy, skoro TV nigdy nie dorówna podaży – komora nigdy nie może być w całości opróżniona. Z wdechu na wdech resztki aerozolu rozpraszają się w tej nieosiągalnej dla poboru przestrzeni tworząc ciąg rozcieńczeń, który od nieskończonego malejącego ciągu znanego z matematyki różni się jedynie policzalną liczbą niepodzielnych w rzeczywistości cząstek aerozolu. Porównanie przykładów 7C i 8C uczy nas, że przy uwzględnieniu dyfuzji część masy (czytaj część dawki) „zawracana jest” i „miksowana” z powietrzem dopełniającym. W sytuacji 7D do pobrania przygotowany jest krótszy blok nierozcieńczonego aerozolu, podczas gdy w przykładzie 8D pobrać trzeba nieosiągalną objętość rozcieńczonego aerozolu. W przykładzie 7E algorytm kończył kalkulację przyjmując, że cały aerozol został pobrany ale w przykładzie 8E algorytm uwzględniający dyfuzję rozpoznaje stratę dawki zawartej w dyfundujących do powietrza dopełniającego cząstkach aerozolu.
PODSUMOWANIE
Nie jest prawdą, że w aspekcie kalkulacji dawek dostarczanych i deponowanych terapia z wykorzystaniem pMDI i komór inhalacyjnych rządzi się innymi prawami. Przeciwnie – co do istoty problemu w obu przypadkach many do czynienia ze stratami w czasie wdechu (nadmiarowość podaży) oraz stratami w czasie wydechu (czas połowicznego zaniku w KI lub nieefektywna emisja w nebulizacji).
Nie jest prawdą, że opis strony sprzętowej terapii z wykorzystaniem pMDI jest prosty a w przypadku skomplikowany. Przeciwnie – w obu przypadkach mamy do czynienia z niezwykle zbieżnymi zjawiskami i ewidentnymi analogiami:
| nebulizacja | pMDI z komorą inhalacyjną |
|---|---|
| dawka możliwa do wyemitowania zależna od strat w przestrzeni martwej NRV | dawka możliwa do wyemitowania zależna od strat w mechanizmie impaktu |
| dawka możliwa do dostarczenia w fazie wdechu zależna od proporcji emisji AO do zdolności poboru TV | dawka możliwa do dostarczenia w fazie wdechu zależna od proporcji objętości KI do zdolności poboru TV |
| straty w fazie wydechowej związane z nieefektywną emisją | straty w fazie wydechowej związane z czasem połowicznego zaniku aerozolu |
| dawka deponowana powiązana z FPF | dawka deponowana powiązana z FPF |
| dawka skumulowana zależna od w/w oraz liczby wdechów | dawka skumulowana zależna od w/w oraz liczby wdechów |
Pomimo forsowania pMDI + KI jako metody z wyboru w terapii wziewnej w miejsce nebulizacji nie jest prawdą, że argumentacja za/przeciw każdej z metod ma podobną rangę merytoryczną. Przeciwnie – w przypadku nebulizacji dysponujemy w praktyce spójnym zastawem parametrów opisanych w instrukcji obsługi inhalatorów podczas gdy w metodzie pMDI + KI nie dysponujemy żadnymi danymi na poziomie praktycznym. Wymieńmy kilka istotnych:
| nebulizacja | pMDI z komorą inhalacyjną |
|---|---|
| ciśnienie robocze sprężarki znane, stałe, niezależne od temperatury | silna zależność ciśnienia w funkcji temperatury, jednak ciśnienie robocze nie podawane przez producenta |
| prędkość liniowa aerozolu natywnego możliwa do wyliczenia z wzoru na przepływ objętościowy Q=v*S | prędkość liniowa aerozolu nie podana przez producenta a z powodu barku innych istotnych danych fizycznych niemożliwa do oszacowania |
| znana na podstawie podanego parametru przepływu objętość aerozolu | objętość produkowanego aerozolu natywnego nie podana przez producenta |
| aerozol „natywny” podawany bezpośrednio do dróg oddechowych, zjawiska depozycji zachodzą jednokrotnie w drogach oddechowych | aerozol „natywny” podawany wstępnie do KI, zjawiska depozycji zachodzą dwukrotnie: w komorze inhalacyjnej a następnie w drogach oddechowych |
| frakcja cząstek drobnych FPF znana i podana przez producenta podawana „taka jaka jest” do dróg oddechowych pacjenta | frakcja cząstek drobnych FPF nieznana, brak danych producenta, wtórna modyfikacja FPF w mechanizmie separacji, nieznana FPF w aerozolu opuszczającym KI |
| losy aerozolu w maseczce: aerozol usunięty z maseczki w czasie wydechu zastępowany nowym aerozolem; proces o znanym tempie zależnym od AO i LO | losy aerozolu w maseczce: po usunięciu w fazie wydechu nie jest zastępowany nowym aerozolem |
| losy aerozolu w kolejnych wdechach: każdy kolejny wdech ma szansę na pobranie dokładnie opisanego (LO,AO,FPF), stabilnego, jednorodnego aerozolu | losy aerozolu w kolejnych wdechach: każdy kolejny wdech pobiera aerozol o nieznanej, malejącej gęstości związanej z z czasem zaniku połowicznego i postępującym rozcieńczeniem (nie dotyczy sytuacji, gdy TV>VKI) |
WNIOSKI
Rodzi się wątpliwość i obawa, czy fascynacja metodą inhalacji z wykorzystaniem dozowników pMDI i komór inhalacyjnych nie wynika ze zbyt powierzchownego postrzegania jej istoty i licznych kluczowych dla efektywności leczenia zależności. Wydaje się, że odbrązowienie, sprowadzenie (ale nie strącenie) z piedestału i wyprowadzenie tej metody z oparów kadzidła do obszaru zdrowej, rzeczowej i racjonalnej refleksji może być kluczem do sukcesów w jej zastosowaniach praktycznych. Warto zdaniem autora prześledzić różne konstelacje znanych i domniemanych parametrów, poeksperymentować wirtualnie z doborem komór i maseczek u dzieci i niemowląt by w efekcie „wykrzesać” z tej wartościowej skądinąd metody poziom dawkowania dużo wyższy od żenujących ułamków procenta dawki deponowanej1).
Kliknij obrazek by przejść do strony z aplikacją on-line