➀ Płytki wdech TV 0,25 L z poprawnym wyzwoleniem dawki pMDI vs. nebulizacja TV 0,25 L vs. nebulizacja TV 0,25 L nadzorowana elektronicznie. ➁ Wdech TV 0,5 L z poprawnym wyzwoleniem dawki pMDI vs. nebulizacja TV 0,5 L vs. nebulizacja TV 0,5 L nadzorowana elektronicznie. ➂ Wdech TV 0,75 L z poprawnym wyzwoleniem dawki pMDI vs. nebulizacja TV 0,75 L vs. nebulizacja TV 0,75 L nadzorowana elektronicznie. ➃ Wdech TV 4,11 L z poprawnym wyzwoleniem dawki pMDI vs. nebulizacja TV 4,11 L vs. nebulizacja TV 4,11 L nadzorowana elektronicznie. ➄ Konkluzja z symulacji. ▷
Jak wiadomo, technika pMDI jest techniką „impulsową”, to znaczy, że dawka jest wyzwalana i dostępna w bardzo krótkim, jednorazowo pojawiającym się przedziale czasowym. W powszechnej opinii problem z dozownikami pMDI stosowanymi samodzielnie wiąże się z koniecznością bardzo dobrej synchronizacji wyzwolenia dawki z początkiem wdechu. Czy rozwiązanie tej kwestii czyni automatycznie z techniki pMDI technikę wiodącą?
Dozownik pMDI stosowany w trakcie płytkiego wdechu.
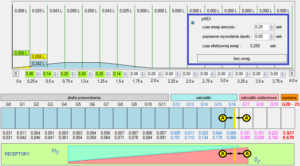
Ryc. 1. Napełnianie dróg oddechowych objętością 250 ml i lokowaniem chmury z dozownika pMDI.
Na rycinie powyżej zilustrowano losy aerozolu wyzwalanego z urządzenia pMDI. Jak wiadomo, jednym z głównych celów udostępnienia KONTEKSTERA jest pomoc w wyrabianiu sobie swego rodzaju „dyscypliny intelektualnej” i nawyku logicznego myślenia o aerozoloterapii. W związku z powyższym na wstępie należy zadać sobie pytanie, jak do płytkiego wdechu pacjenta ma się objętość aerozolu produkowanego z pMDI? Okazuje się, że w czasie 0,25 sek, czyli w czasie emisji aerozolu pacjent pobiera około 0,008 litra powietrza. Wyprodukowany aerozol ma natomiast objętość około 0,028 litra, czyli ponad trzykrotnie większą. W układzie otwartym, jakim jest technika inhalacji pMDI bez komory inhalacyjnej prawdopodobieństwo, że na skutek chwilowego nadciśnienia 2/3 aerozolu wydostanie się poza układ oddechowy a jedynie 0,008 L aerozolu podąży w jego głąb jest bardzo wysokie. Nie ma możliwości rzetelnej odpowiedzi na pytanie, co dzieje się z aerozolem w trakcie jego wędrówki prze kolejne generacje drzewa oskrzelowego, można jednak porównać sytuacje, w których analizujemy stan statyczny: obraz aerozolu i powietrza dopełniającego w momencie zatrzymania wdechu.
Ryc. 2. Napełnianie dróg oddechowych objętością 250 ml i lokowaniem chmury aerozolu nebulizowanego.
Takie rozumowanie pozwala na wskazanie kardynalnej różnicy metodologicznej w ocenie porównawczej techniki pMDI oraz nebulizacji, mianowicie w przypadku pMDI dyskusję rozpoczynamy od spekulacji na temat, co działo się w przeszłości, w momencie przechodzenia aerozolu w obszarze, w którym obecnie go nie ma oraz losów chmury zatrzymanej w obrębie 16 generacji oskrzeli w chwili obecnej, porównywanej. W przypadku nebulizacji, techniki opartej na emisji ciągłej, mamy pewność, że w chwili zatrzymania wdechu, poza śladami przejścia czoła chmury aerozolu, co do losów których możemy również jedynie spekulować, obecna jest z całą pewnością objętość aerozolu podlegająca prawom depozycji. Innymi słowy, obie porównywane techniki są bardzo podobne pod względem prawideł rządzących depozycją dynamiczną płynącego przez drzewo oskrzelowe aerozolu, jednak w przypadku nebulizacji may do czynienia z ewidentną wartością dodaną: aerozolem obecnym przy zatrzymaniu wdechu i podlegającym dodatkowej depozycji w myśl praw depozycji statycznej. Porównując ryc. 1 i 2 staje się jasne, że dwa efekty deponowania aerozolu w szerszym obszarze możliwe są jedynie w przypadku nebulizacji. Jej wadą w przypadku inhalatorów klasycznych jest depozycja w obrębie przestrzeni martwej i obszarze przewodzeniowym.
Ryc. 3. Niwelowanie depozycji w obszarze przewodzenia z szerokim obszarem zalegania aerozolu po zatrzymaniu wdechu.
Na rycinie 3 ukazano modyfikację nebulizacji poprzez wykorzystanie nadzoru elektronicznego. Rezultatem jej jest znaczne poszerzenie obszaru „depozycji statycznej” z eliminacją aerozolu ze strefy przewodzenia.
Dozownik pMDI stosowany w trakcie wdechu TV rzędu 0,5L .
Ryc. 4. Lokalizacja chmury aerozolu z pMDI przy wdechu o TV rzędu 0,5 L.
Wdech nieco głębszy, o objętości rzędu 0,5L pozwala na wygenerowanie w pierwszych o,25 sek wdechu przepływów, a zatem i odpowiadających im objętości około 19 ml, co stanowi niespełna 70% objetości pojawiającego się aerozolu. Jest to wynik lepszy niż w przypadku wdechu ilustrowanego na ryc. 1.
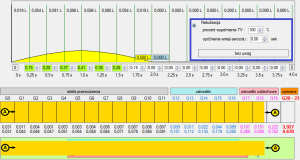
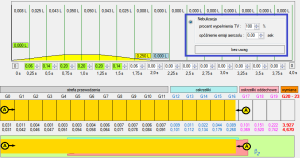
Ryc. 5. Napełnianie dróg oddechowych objętością 500 ml i lokowaniem chmury aerozolu nebulizowanego.
Jak to omawiano wyżej, nebulizacja gwarantuje obecność aerozolu w drogach oddechowych w obszarze znacznie większym niż ten, jaki jest w stanie zagospodarować aerozol z pMDI.
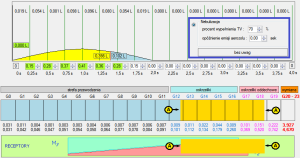
Ryc. 6. Niwelowanie depozycji w obszarze przewodzenia przy wykorzystaniu elektronicznego nadzoru nad nebuizacją.
Dozownik pMDI stosowany w trakcie wdechu TV rzędu 0,75L .
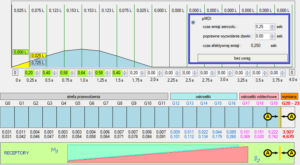
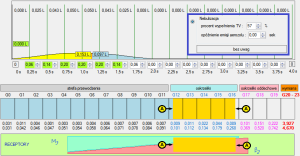
Ryc. 7. Poprawa efektywności poboru dawki z pogorszeniem lokalizacji docelowej chmury przy głębszym wdechu.
Wdech o objętości 0,75 L wykonywany w przeciągu 2 sekund pozwala na niemal pełne zagospodarowanie dawki wyzwalanej z pMDI (ok. 25 ml/0,25 sek vs ok. 28ml/0,25 sek). Niestety, poprawie tej towarzyszy nieuchronne przesunięcie lokalizacji miejsca zatrzymania chmury w kierunku strefy wymiany gazowej (Ⓐ→ G19 ←Ⓐ).
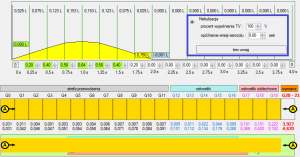
Ryc. 8. Napełnianie dróg oddechowych objętością 750 ml i lokowaniem chmury aerozolu nebulizowanego.
Rycina 8 ilustruje tezy omawiane powyżej: nie gorszy niż przy pMDI „zasięg” aerozolu wgłąb drzewa oskrzelowego, gwarancję jego obecności w licznie reprezentowanych generacjach dróg oddechowych oraz, niestety, jego nadmiarowość w strefie martwej i przewodzenia.
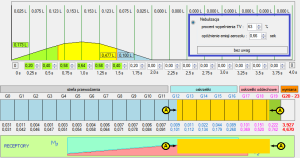
Ryc. 9. Nadzór elektroniczny nad nebulizacją: optymalizacja przejścia i zatrzymania chmury aerozolu w obszarze docelowym.
Dozownik pMDI stosowany w trakcie wdechu o TV bliskiej VC .
Wiele zaleceń opisuje technikę inhalacji z pMDI wskazując na konieczność wstępnego opróżnienia płuc. Manewr taki, zilustrowany w artykule o objętościach oddechowych, oznacza wprost posługiwanie się objętością TV bliską pojemności życiowej VC. Jak w takich warunkach przebiegać może inhalacja z pMDI?
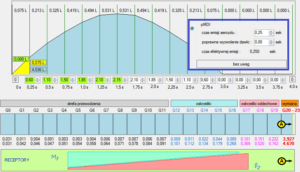
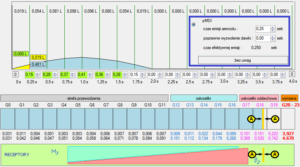
Ryc. 10. Wysokie, graniczące z VC objetości wdechu i ich konsekwencje dla lokalizacji chmury aerozolu z pMDI.
Jak wynika z obliczeń przedstawionych na rycinie 10, po pierwsze: objętość powietrza pobierana w pierwszej , liczącej 0,25 sek fazie wdechu jest tym razem ponad dwukrotnie większa od niezbędnej dla bezstratnego poboru aerozolu, po drugie: cała objętość chmury lokowana jest w głębokich obszarach strefy wymiany gazowej. Po raz drugi powracam do kwestii niedostatków rzetelnej wiedzy na temat losów aerozolu w inhalacji techniką pMDI. Dostępne dane są często przedstawiane hasłowo i nierzadko traktowane instrumentalnie w celu forsowania wycinkowego aspektu wiedzy. Jednym z intensywnie wykorzystywanych haseł jest poprawa depozycji płucnej w przypadku aerozoli drobnocząsteczkowych. Istota tej tezy sprowadza się do twierdzenia, że im mniejsza jest MMAD aerozolu, tym lepsza jest obwodowa depozycja aerozolu. Co oznacza to dla omawianego „kontekstu dawki”? Okazuje się, że jeśli przyjmiemy konsekwentnie teorię o związku niskiej MMAD i depozycji obwodowej i nie będziemy traktować jej wybiórczo i instrumentalnie, wówczas stajemy przed paradoksem polegającym na tym, że poprawa cech aerozolu ( niskie MMAD) łączy się ze wzrostem ryzyka działań systemowych, tez kolei są tym bardziej prawdopodobne, im bliżej pęcherzyków płucnych dociera aerozol. Próba obrony dobrej depozycji w obszarach poprzedzających strefę wymiany gazowej z wykorzystaniem argumentu o szerszej rozpiętości GSD jest bronią obosieczną. Z jednej strony uzasadnia wzrost depozycji cząstek większych od MMAD „po drodze” ku pęcherzykom płucnym, z drugiej strony oznacza nie mniej, nie więcej, jak większy odsetek cząstek dużo mniejszych od MMAD i lepszą penetrację do pęcherzyków płucnych.
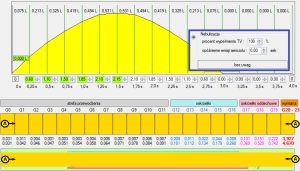
Ryc. 11. Napełnianie dróg oddechowych objętością 4,44 L i lokowaniem chmury aerozolu nebulizowanego.
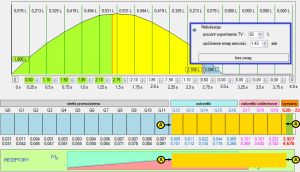
Ryc. 12. Niwelowanie depozycji w obszarze przewodzenia i strefie wymiany gazowej dzięki elektronicznej kontroli nebulizacji.
Na rycinach 11 i 12 ukazano dramatyczną różnicę w zakresie zastosowania nebulizacji vs. techniki pMDI. Jak na rycinach poprzednich, aerozol jest trwale obecny we wszystkich kluczowych dla terapii strefach a elektroniczna kontrola jego dystrybucji pozwala na zniwelowanie licznych wątpliwości metodologicznych i teoretycznych, które napotykamy borykając się z faktycznym opisem losów aerozolu podawanego z pMDI.
Desynchronizacja wdechu
Dla porządku i rzetelności wykładu problemu należy wskazać również sytuacje, w których technika pMDI prezentuje zachowanie bardziej przystające do oczekiwań wobec metody skutecznego i przewidywalnego podawania aerozolu. Co ciekawe, spełnienie tychże oczekiwań wiąże się z istotnym odstępstwem od powszechnie utrwalonych poglądów i opinii na temat synchronizacji wyzwolenia dawki z początkiem wdechu.
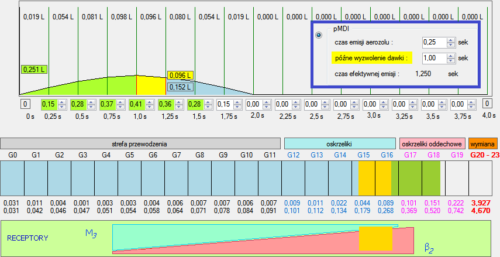
Ryc. 13. Efekt poprawnej lokacji aerozolu na końcu wdechu poprzez radykalne opóźnienie wyzwolenia dawki.
W sytuacjach szczególnych, to znaczy dla konkretnego układu zmiennych opisujących objętość wdechową TV, czas trwania wdechu i opóźnienie wyzwolenia dawki można uzyskać korzystną lokalizację końcową chmury a w efekcie możliwość zastosowania nie tyle bardziej spójnej, co mniej spekulatywnej koncepcji depozycji w obszarze docelowym.
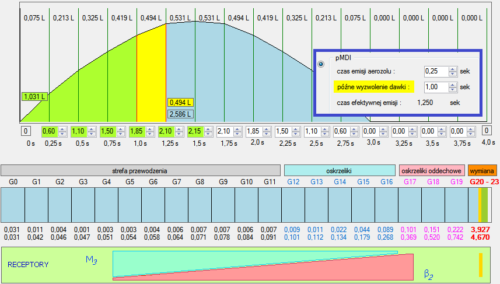
Ryc. 14. Nikła poprawa lokalizacji przy dużych, sięgających 1-2 sekund opóźnieniach emisji z pMDI przy dużych objętościach wdechowych.
Niestety, w przypadku oddychania dużymi objętościami wdechowymi nawet radykalne, trwające do 2 sekund opóźnienie momentu początku emisji aerozolu nie przynosi oczekiwanego efektu.
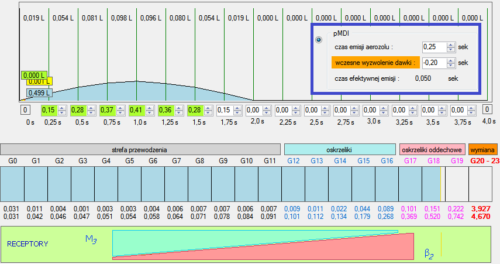
Ryc. 15. Zbyt wczesne wyzwolenie dawki praktycznie wyklucza penetrację aerozolu do dolnych dróg oddechowych.
Prezentowane na rycinie 13, jednosekundowe, a więc znaczne opóźnienie wyzwolenia dawki z pMDI w stosunku do początku wdechu poprawiało efektywność inhalacji. Wystarczy jednak drobna, o,2 sekundowa desynchronizacja ze zbyt wczesnym wyzwoleniem aerozolu, by zniweczyć szanse na dostarczanie aerozolu w obręb dolnych dróg oddechowych pacjenta.
WNIOSKI Z SYMULACJI
- w przeciwieństwie do nebulizacji technika pMDI jest podatna na czynniki utrudniające poprawne dawkowanie leku zależne od sposobu oddychania pacjenta w czasie emisji aerozolu.
- desynchronizacja wdechu, krytyczna w przypadku techniki pMDI z definicji nie ma odniesienia do nebulizacji
- nebulizacja pozwala na redukcję ryzyka nadprodukcji aerozolu1) w pierwszych chwilach wdechu
- rozpatrując mechanizmy osadzania cząstek leku w obszarze Ⓐ→ G12 – G18 ←Ⓐ , a więc w strefach kluczowych dla kontroli przepływu i redukcji stanu zapalnego, w przypadku nebulizacji mają zastosowanie dwie koncepcje depozycji, natomiast przy pMDI nie może być mowy o obecności aerozolu w tym obszarze w momencie zakończenia wdechu
- elektroniczna kontrola nebulizacji eliminuje niedoskonałości nebulizacji klasycznej.
